Es aquel en el cual una o más sustancias en estado sólido,
líquido o gaseoso, llamadas fase dispersa, se encuentran disueltas en otra
sustancia, llamada fase dispersora. Los sistemas dispersos se encuentran en
todas partes, por ejemplo el agua en las nubes, la sangre y líquidos
corporales. La clasificación de un sistema disperso se basa en el tamaño de las
partículas de la fase dispersa, pudiendo agruparse básicamente en tres tipos:
soluciones, coloides y suspensiones.
Disoluciones:
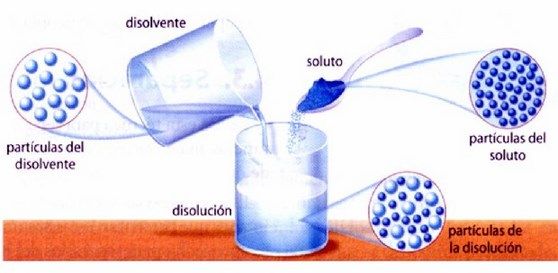 Definición: Es una mezcla homogénea de dos o más sustancias en proporción variable, en las disoluciones la sustancia que se encuentra en mayor proporción
Definición: Es una mezcla homogénea de dos o más sustancias en proporción variable, en las disoluciones la sustancia que se encuentra en mayor proporción
(fase dispersora) se llama solvente o disolvente, y la que se encuentra en menor proporción (fase dispersa ) se llama soluto. Se presentan en tres estados de agregación, el cual determina el disolvente.
Características:
- Tamaño de la partícula del soluto menor a 1nm.
- Homogeneidad
- Transparencia
- Filtrabilidad (partículas que pasan a través de cualquier filtro)
- Las propiedades coligativas varían con la concentración
- Sus partículas no sedimentan.
Ejemplos:
Aleaciones metálicas, amalgamas, paladio hidrogenado, salmuera, agua de mar, vinagre, bebidas alcohólicas, anticongelante, refrescos gaseosos, sidras, humo, brisa marina, humedad, helio en oxígeno, aire, gas L.P , etc.
Solubilidad:
Es una propiedad de los solutos. Se refiere a la cantidad de sustancia que puede disolverse en una determinada cantidad de disolvente, bajo condiciones de temperatura y presión específicas.
Propiedades coligativas: Efecto colectivo de las partículas del soluto sobre el disolvente, estas propiedades son cuatro: presión de vapor, punto de ebullición,punto de congelación y ósmosis.
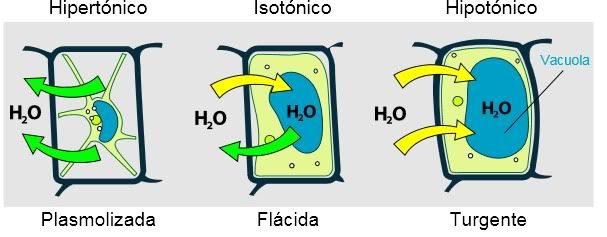
Tipo de disoluciones:
◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄◄
Coloides
Características:
- Tamaño de las partículas coloidales de 1-1000nm
- Apariencia homogénea en microscopio heterogénea
- Sus partículas pueden sedimentar después de mucho tiempo
- Presentan efecto Tyndall
- Presentan movimiento Browniano
- Pueden presentar el fenómeno de floculación y adsorción.
Efecto Tyndall: Es un fenómeno que se aprecia cuando un rayo de luz pasa por una mezcla coloidal y este es reflejado por las partículas.
Movimiento Browniano: movimiento de las partículas en zig-zag, por las colisiones entre las moléculas.
Floculación: Proceso instantáneo entre las partículas de los coloides para alcanzar un mayor tamaño, por ejemplo cuando se añade limón a la leche y esta se corta, este fenómeno permite la elaboración de queso, mantequilla, yogurth, etc.
Adsorción: Esta característica es importante en la elaboración de filtros para el agua, ya que contiene carbón activado
Ejemplos de coloides:




No hay comentarios:
Publicar un comentario